Qu'est-ce que Enhertu? | Informations et FAQ
Dernière mise à jour : 14 octobre 2022
Vous pouvez accéder légalement à de nouveaux médicaments, même s'ils ne sont pas approuvés dans votre pays.
En savoir plus "Article revu par le Dr Jan de Witt
Qu'est-ce que Enhertu?
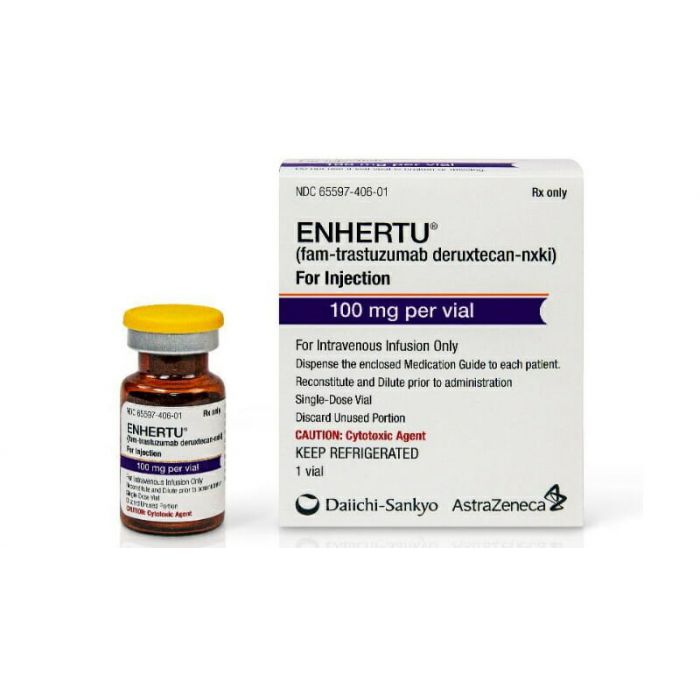
Enhertu (fam-trastuzumab deruxtecan-nxki) est une thérapie ciblée par conjugaison anticorps-médicament indiquée pour le traitement des personnes atteintes de.. :
- Cancer du sein HER2-positif non résécable ou métastatique ayant reçu au moins deux thérapies antérieures pour leur cancer métastatique.
- Adénocarcinome gastrique ou de la jonction gastro-oesophagienne (GEJ) localement avancé ou métastatique HER2 positif ayant reçu un traitement antérieur à base de trastuzumab.
Il est disponible sous forme de flacon monodose contenant chacun 100 mg de fam-trastuzumab deruxtecan-nxki.12
Enhertu (fam-trastuzumab deruxtecan-nxki) est un médicament utilisé pour le traitement des patients adultes atteints d'un cancer du sein HER2 positif non résécable ou métastatique précédemment traité ou d'un cancer gastrique HER2 positif avancé.
Combien coûte le site Enhertu ?
Pour plus d'informations sur Enhertu et sur la manière dont nous pouvons vous aider à y accéder, cliquez sur le bouton ci-dessous :
Est-ce que Enhertu est un médicament de chimio ?
Oui, Enhertu est un médicament de chimio. C'est également un médicament d'immunothérapie ciblée. Les médicaments de chimiothérapie empêchent les cellules cancéreuses de se développer et de se propager en les détruisant ou en les empêchant de se diviser. Enhertu a été fabriqué en associant deux types différents de médicaments anticancéreux pour en faire un médicament appelé conjugué anticorps-drogue (ADC). 3
Est-ce que Enhertu est une immunothérapie ?
Oui, Enhertu est également un médicament d'immunothérapie ciblée. Les médicaments d'immunothérapie utilisent le système immunitaire de l'organisme pour combattre les cellules cancéreuses en stimulant les défenses naturelles du système immunitaire de l'organisme. 4
Comment le site Enhertu est-il administré ?
La posologie standard pour Enhertu est de 5,4 mg/kg de poids corporel une fois toutes les 3 semaines (cycle de 21 jours).
Il est administré en perfusion intraveineuse pendant 90 minutes. Si elle est bien tolérée, les perfusions suivantes peuvent être administrées sur 30 minutes. Une réduction de la dose peut être nécessaire en fonction des symptômes et des effets secondaires ressentis. Ne pas augmenter la dose de Enhertu après une réduction de la dose.
Vous trouverez des informations complètes sur la posologie et l'administration de Enhertu (fam-trastuzumab deruxtecan-nxki) dans les informations de prescription officielles figurant dans notre section Références.1
Le site Enhertu provoque-t-il la chute des cheveux ?
Les effets secondaires les plus courants ( ≥20% des patients) mentionnés dans les informations de prescription sont les suivants : 1
- Nausées
- Fatigue
- Vomissements
- Chute de cheveux
- Constipation
- Diminution de l'appétit
- Un faible taux de globules rouges et/ou blancs
- Faible nombre de plaquettes
- Diarrhée
- Toux
Les effets indésirables graves énumérés dans les informations de prescription sont notamment les suivants
Enhertu (fam-trastuzumab deruxtecan-nxki) peut être fatal pour un fœtus, il est conseillé d'éviter les grossesses et l'allaitement.
Qui fabrique Enhertu?
Enhertu est fabriqué par AstraZeneca et Daiichi Sankyo. AstraZeneca plc est une multinationale anglo-suédoise de l'industrie pharmaceutique et biopharmaceutique dont le siège social se trouve à Cambridge, en Angleterre. Daiichi Sankyo Company, Limited est une entreprise pharmaceutique mondiale et la deuxième plus grande entreprise pharmaceutique du Japon.5
Quand Enhertu a-t-il été approuvé par la FDA ?
Enhertu (fam-trastuzumab deruxtecan-nxki) a été approuvé par :
- Food and Drug Administration (FDA), États-Unis :
- PMDA, Japon, le 25 mars 2020 pour le traitement des patientes atteintes d'un cancer du sein HER2 positif non résécable ou récidivant après une chimiothérapie antérieure (limiter l'utilisation aux patientes réfractaires ou intolérantes aux traitements standard).
Le 20 décembre 2019 avec une approbation accélérée pour le traitement des patients adultes atteints d'un cancer du sein HER2 positif non résécable ou métastatique qui ont reçu deux ou plusieurs traitements antérieurs à base d'anti-HER2 en milieu métastatique. 1
Le 15 janvier 2020 pour les patients ayant déjà été traités pour un cancer gastrique métastatique HER2-positif.
La FDA a accordé à Enhertu la désignation Breakthrough Therapy et Orphan Drug Designation pour le traitement des patients atteints d'un cancer gastrique HER2-positif avancé, et le produit fait actuellement l'objet d'une évaluation prioritaire pour cette indication.
Enhertu a également reçu la désignation Breakthrough Therapy pour le traitement du cancer du poumon non à petites cellules métastatique HER2-mutant. 5
Références :
- Access.fda.gov
- Reuters.com
- ِِEnhertu - Breastcancer.org
- Immunothérapie - Cancer du sein.org
- Enhertu (fam-trastuzumab deruxtecan-nxki)- Thesocialmedwork.com